28/07/2022
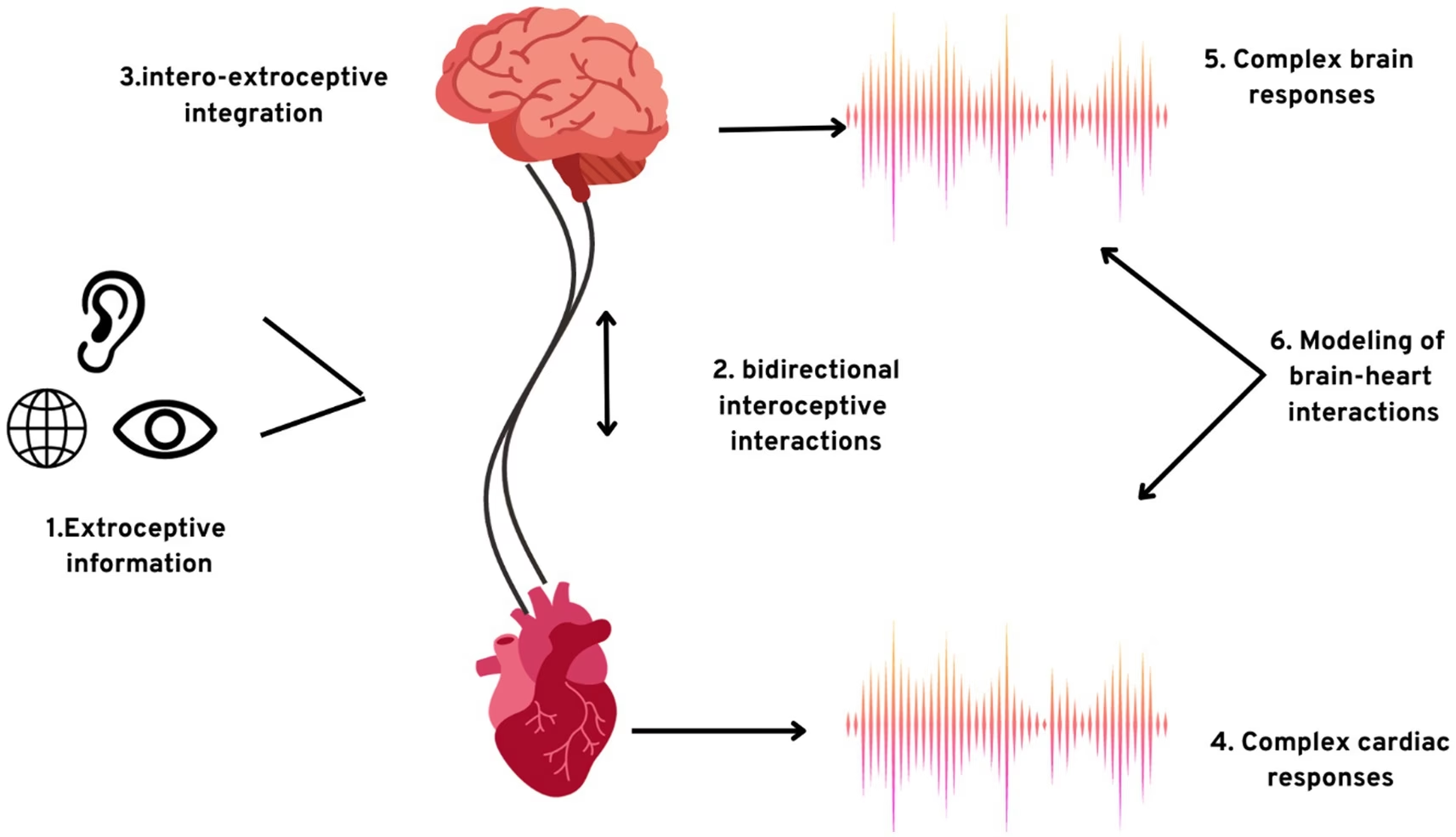
Corpul uman este o mașinărie complexă, iar inima, motorul său neobosit, este reglată de o rețea intricată de mecanisme neurale. Aceste mecanisme, cunoscute sub denumirea de reflexe cardiovasculare, joacă un rol vital în menținerea echilibrului fiziologic, adaptând funcția cardiacă la cerințele fluctuante ale organismului. De la răspunsurile rapide la exerciții fizice intense, la adaptările subtile din timpul somnului sau al stresului emoțional, aceste reflexe sunt esențiale pentru supraviețuire și bunăstare. În acest articol, vom explora în profunzime câteva dintre cele mai importante reflexe cardiovasculare, modul în care acestea funcționează și implicațiile lor clinice, oferind o perspectivă cuprinzătoare asupra modului în care sistemul nervos controlează inima.
- Reflexul Trigemenocardiac (TCR): O Conexiune Surprinzătoare
- Reflexul Presor la Exercițiu și Comanda Centrală: Reglarea Hemodinamică
- Baroreflexul Arterial: Păstrătorul Echilibrului Tensional
- Simpatoexcitația și Repolarizarea Ventriculară: Impactul Asupra Aritmiilor
- Implicații Clinice ale Modulării Simpatice
- Direcții Viitoare în Modularea Simpatică
- Întrebări Frecvente (FAQ)
- Concluzie
Reflexul Trigemenocardiac (TCR): O Conexiune Surprinzătoare
Reflexul trigemenocardiac (TCR) este definit ca debutul brusc al unei disritmii parasimpatice, hipotensiunii simpatice, apneei sau hipermotilității gastrice, declanșat de stimularea ramurilor senzoriale ale nervului trigemen. Acest reflex, deși adesea asociat cu intervențiile chirurgicale cranio-faciale, are o importanță fiziologică mult mai largă, influențând diverse condiții neurologice și chiar reacțiile de conservare a oxigenului.
Arcul reflex propus implică stimularea terminațiilor nervoase senzoriale – ramurile senzoriale ale nervului trigemen – care transmit semnale neuronale către nucleul senzorial al nervului trigemen prin ganglionul Gasserian, formând calea aferentă a arcului reflex. Fibrele nervoase internunciale din formațiunea reticulară conectează nucleul senzorial al nervului trigemen la nucleul motor al nervului vag, care, împreună cu nucleul său motor, formează calea eferentă a arcului reflex. Această conexiune directă explică de ce stimularea trigeminală poate avea efecte atât de profunde asupra funcției cardiace.
TCR a fost raportat în numeroase situații clinice, inclusiv în timpul chirurgiei cranio-faciale, chirurgiei transsfenoidale, rizolizei ganglionului trigeminal și manipulării nervului trigemen. Prezența sa poate duce la manifestări clinice variate, de la bradicardie și hipotensiune până la asistolă completă și/sau apnee. Datorită acestor complicații potențial letale, TCR a atras o atenție enormă și crescândă în ultimii ani.
Importanța fiziologică a TCR a fost, de asemenea, raportată. Studiile experimentale sugerează că reflexul reprezintă o expresie a unui reflex neurogenic central care duce la vasodilatație cerebrovasculară rapidă, generată de excitarea neuronilor sensibili la oxigen din medula oblongată ventrolaterală rostrală. Prin acest răspuns fiziologic, se inițiază ajustări ale circulației sistemice și cerebrale pentru a devia sângele către creier sau pentru a crește fluxul sanguin în interiorul acestuia. Se acceptă în general că reflexul de scufundare și toleranța la ischemie implică mecanisme fiziologice cel puțin oarecum similare. Prezența unor astfel de mecanisme neuroprotective endogene poate extinde spectrul TCR dincolo de apariția sa clinică cunoscută, pentru a include și prevenirea altor stări potențiale de leziuni cerebrale.
TCR în Diverse Condiții Non-Chirurgicale
- Bruxismul de Somn: Această tulburare de somn, caracterizată prin încleștarea sau scrâșnirea dinților în timpul somnului, este asociată cu activitate intensă de trezire în timpul somnului (microarousal). Stimularea mușchilor masticatori faciali inițiază TCR, ducând la o încetinire a ritmului cardiac. Contactul dintre dinți stimulează, de asemenea, mecanoreceptorii din țesutul periodontal pentru a iniția TCR și bradicardia. Astfel, bruxismul de somn poate fi considerat o formă de autoreglare, protejând corpul de apariția tahicardiei în timpul somnului prin stimularea nervului trigemen.
- Reflexul de Scufundare: Acest mecanism reflex, moștenit probabil de la păsările acvatice și amfibieni, persistă la om. Activități precum spălarea feței cu apă rece sau scufundarea în apă rece pot provoca o scădere a ritmului cardiac prin stimularea ramurilor nervului trigemen de pe față. Reflexul de scufundare este un subtip periferic al TCR, caracterizat prin bradicardie, apnee și vasoconstricție periferică cu o creștere treptată a tensiunii arteriale. Funcțional, acest reflex a fost demonstrat ca un mecanism de conservare a oxigenului, redistribuind debitul cardiac către organele vitale precum creierul și inima.
- Spasmul Arterial Coronarian: Deși tulburările hemodinamice din timpul intervențiilor neurochirurgicale sunt adesea atribuite stimulării vagale, reflexul vagal este o parte a TCR. Ori de câte ori stimularea chirurgicală are loc în apropierea nervului trigemen sau a durei mater, TCR poate fi incitat, ducând la modificări cardiovasculare. Studiile experimentale sugerează că TCR-ul duce la vasodilatație cerebrovasculară rapidă și crește perfuzia cerebrală, sugerând că spasmul arterial coronarian mediat de TCR ar putea acționa ca un mecanism cardioprotector.
Reflexul Presor la Exercițiu și Comanda Centrală: Reglarea Hemodinamică
În timpul exercițiilor dinamice intense, cum ar fi alergarea sau ciclismul, are loc o reducere semnificativă a rezistenței vasculare sistemice din cauza vasodilatației metabolice intense în musculatură. Aceasta ar putea provoca o scădere periculoasă a tensiunii arteriale dacă mecanismele de control nu ar crește concomitent debitul cardiac. Reglarea fină a hemodinamicii în timpul efortului este determinată de activitatea a trei mecanisme neurale principale: reflexul presor la exercițiu, comanda centrală și baroreflexul arterial.
Reflexul Presor la Exercițiu: Senzori Musculari și Răspuns Cardiac
Acest reflex provine din semnale periferice generate de mecano- și metaboreceptori (terminații nervoase de tip III și IV din mușchi) care modulează reflexiv activitatea simpatică, ținând cont de condițiile mecanice și metabolice din mușchiul în lucru. Terminatiile nervoase de grup III acționează predominant ca mecanoreceptori, iar cele de grup IV ca metaboreceptori, deși ambele tipuri pot acționa dual. Acestea colectează informații despre condițiile mecanice și metabolice ale mușchilor contractanți și le transmit centrelor de control cardiovascular din măduva spinării și creier, unde informațiile sunt integrate și elaborate pentru a organiza răspunsul hemodinamic la efort.
Substanțe precum acidul lactic, potasiul, bradikinina, ATP-ul și adenozina pot activa metaboreflexul. Acesta este activat ori de câte ori fluxul sanguin către mușchii contractanți este insuficient pentru a asigura livrarea de oxigen și/sau eliminarea metaboliților, sugerând că acest reflex corectează orice posibilă nepotrivire între fluxul sanguin și metabolismul muscular. Consecința tipică a recrutării metaboreflexului este o creștere a tensiunii arteriale medii (MAP), realizată prin modularea atât a rezistenței vasculare sistemice (SVR), cât și a debitului cardiac (CO).
Comanda Centrală: Impulsul Voluntar al Efortului
Comanda centrală este un mecanism feed-forward care implică activarea paralelă a centrelor motorii și cardiovasculare. Acest mecanism nu necesită feedback din partea mușchilor periferici. Impulsurile neurale din cortexul motor iradiază către neuronii autonomi din trunchiul cerebral, stabilind, la începutul exercițiului, un nivel de bază al activității eferente simpatice și parasimpatice, strâns legat de intensitatea efortului. Această activitate autonomă de bază este apoi modulată de activarea reflexului presor la exercițiu.
Deși situl cortical precis care subservește acest mecanism rămâne neclar, s-a demonstrat că regiunile premotorii și ariile motorii suplimentare sunt implicate. Comanda centrală crește rapid ritmul cardiac și tensiunea arterială la începutul exercițiului, în principal prin creșterea tonusului simpatic și scăderea tonusului parasimpatic.
Iată o comparație a rolurilor cheie ale mecanoreflexului și metaboreflexului:
| Caracteristică | Mecanoreflex | Metaboreflex |
|---|---|---|
| Stimul principal | Modificări mecanice (contracție, întindere musculară) | Acumularea de metaboliți (acid lactic, K+, ATP etc.) |
| Tipul de fibre aferente | Predominant tip III | Predominant tip IV |
| Răspuns hemodinamic | Creștere rapidă a HR și TA la începutul exercițiului | Creștere susținută a TA, SVR, CO (mai puțin efect asupra HR în izometrie) |
| Momentul activării | Imediat la debutul contracției | Pe măsură ce metaboliții se acumulează (întârziat) |
| Rol fiziologic | Pregătirea rapidă a sistemului CV pentru efort | Asigurarea unui flux sanguin adecvat și eliminarea deșeurilor |
Baroreflexul Arterial: Păstrătorul Echilibrului Tensional
Baroreceptorii arteriali, situați în sinusul carotidian și arcul aortic, sunt esențiali în inducerea ajustărilor rapide ale tensiunii arteriale. Când tensiunea arterială este crescută sau redusă, baroreceptorii sunt întinși sau comprimați, ducând la o creștere sau scădere a frecvenței de descărcare a neuronilor aferenți. Aceste răspunsuri neurale aferente duc la ajustări neurale sistemice mediate reflex, cu modificări ale activităților nervoase simpatice și parasimpatice, care afectează atât circulația centrală (cardiacă), cât și cea periferică (vasele), pentru a readuce tensiunea arterială la punctul său de operare inițial.
Resetarea Baroreflexului în Timpul Exercițiului
S-a demonstrat că baroreflexul arterial este „resetat” în timpul exercițiilor dinamice, funcționând eficient în jurul tensiunii arteriale crescute induse de efort. Această resetare, care implică o deplasare în sus și spre dreapta a curbei stimul-răspuns, permite baroreflexului să opereze la o tensiune arterială mai ridicată, menținând în același timp un control eficient. Importanța acestei resetări este crucială: denervarea acută a baroreceptorilor la animale sau la pacienții umani cu denervare chirurgicală a baroreceptorilor carotidiană duce la o creștere excesivă a tensiunii arteriale în timpul exercițiului. Aceasta demonstrează că baroreflexul acționează pentru a echilibra fin efectele opuse ale vasoconstricției simpatice și vasodilatației metabolice, limitând parțial creșterea tensiunii arteriale.
Simpatoliza Funcțională și Baroreflexul
„Simpatoliza funcțională” este fenomenul prin care activarea simpatică completă este inhibată metabolic în țesutul muscular în exercițiu. Acestă inhibiție metabolică a vasoconstricției simpatice este legată de intensitatea efortului, devenind mai evidentă la eforturi mai mari. Mecanismele simpatolizei funcționale sunt asociate cu producția de metaboliți precum oxidul nitric, adenozina și prostaciclina, precum și cu creșteri ale temperaturii musculare și acidozei metabolice.
În ciuda atenuării răspunsului vascular local la activarea simpatică în mușchiul activ (simpatoliză funcțională), controlul baroreflex al tensiunii arteriale este bine menținut de la repaus la exerciții intense. Acest echilibru permite o creștere continuă a perfuziei mușchiului în exercițiu, împreună cu o capacitate conservată a baroreflexului de a controla conductanța vasculară, ceea ce, în cele din urmă, permite menținerea tensiunii arteriale în timpul exercițiului.
Simpatoexcitația și Repolarizarea Ventriculară: Impactul Asupra Aritmiilor
Dezechilibrul dintre simpatoexcitație și retragerea parasimpatică destabilizează electrofiziologia cardiacă și contribuie la dezvoltarea aritmiilor ventriculare. Simpatoexcitația induce modificări în repolarizarea ventriculară și reduce pragurile de aritmie ventriculară. În inimile explantate de la pacienți cu antecedente de aritmii ventriculare, s-a constatat o creștere a inervației simpatice în zona de graniță a cicatricii și a miocardului supraviețuitor. Mai important, hiperinervația simpatică singură, fără boală coronariană, poate crește susceptibilitatea la aritmii ventriculare.
Neuroanatomia Sistemului Simpatic Cardiac
Sistemul nervos cardiac (CNS) cuprinde componente centrale (Nivelul 3), componente intratoracice extracardiace (Nivelul 2) și sistemul nervos cardiac intrinsec (ICNS) (Nivelul 1). Nivelul 1 reprezintă sistemul „micului creier de pe inimă”, cu plexurile ganglionare rezidând lângă joncțiunea dintre țesutul adipos și miocard. Nivelul 2 include ganglionii cervicotoracici, care conectează componentele centrale și ICNS. Nivelul 3 include ganglionii rădăcinii dorsale, ganglionii nodoși și zonele din măduva spinării și trunchiul cerebral care controlează inima. Neuronii preganglionari simpatici eliberează acetilcolină, care activează neuronii postganglionari ce eliberează norepinefrină, modulând funcțiile fiziologice și electrofiziologice cardiace bătăie cu bătăie.
Evaluarea Funcției Sistemului Nervos Autonom (SNA)
Cu interesul crescând pentru terapia de modulare autonomă, evaluarea funcției SNA a primit atenție:
- Variabilitatea Ritmului Cardiac (HRV): Indică oscilația bătăie cu bătăie a intervalului R-R. Deși odinioară se credea că frecvența joasă (LF) și frecvența înaltă (HF) corespund funcțiilor simpatice, respectiv parasimpatice, studii recente au demonstrat limitările HRV ca indice al funcției SNA.
- Sensibilitatea Baroreflexului (BRS): Este un reflex fiziologic care previne fluctuațiile mari ale tensiunii arteriale pe termen scurt. O BRS redusă a fost asociată cu o susceptibilitate crescută la fibrilația ventriculară și este un predictor independent al mortalității cardiace după infarctul miocardic.
- Turbulența Ritmului Cardiac (HRT): Descrie modul în care ritmul sinusal accelerează și încetinește după o contracție ventriculară prematură. HRT, combinată cu BRS și HRV, poate fi un predictor mai puternic al stopului cardiac.
- Alternanța Undelor T (TWA): Reflectă eterogenitatea sau dispersia în repolarizarea ventriculară. Pacienții cu alternanță electrică de nivel scăzut după infarctul miocardic au un risc mai mare de mortalitate și aritmii ventriculare.
Condiții Situaționale și Aritmiile Ventriculare
- Stresul Emoțional: Stresul emoțional, în special furia și frica, joacă un rol semnificativ în inducerea și terminarea aritmiilor fatale. Mecanismele propuse includ alternarea echilibrului simpatic-parasimpatic, distribuția spațială a inputului autonom cardiac și creșterea catecolaminelor plasmatice.
- Exercițiul Fizic: Antrenamentul fizic este considerat un tratament non-farmacologic eficient pentru bolile cardiovasculare. Se ipotezează că exercițiul ar putea reechilibra sistemele simpatic și parasimpatic. Molecular, exercițiul inhibă hiperfosforilarea RyR2 dependentă de CaMKII, reducând scurgerea de calciu în timpul diastolei și suprimând aritmiile ventriculare. Cu toate acestea, exercițiile cronice de mare intensitate pot fi dăunătoare, cu dovezi de incidență crescută a morții subite cardiace în anumite modalități sportive.
Modularea Proprietăților Electrice Regionale de Simpatoexcitație
Simpatoexcitația crește susceptibilitatea la aritmiile ventriculare prin scurtarea potențialului de acțiune, creșterea eterogenității repolarizării, a calciului intracelular și a postdepolarizării. Aceasta predispune la depolarizări precoce sau tardive. Deși s-a crezut că nervii simpatici inervează ambii ventriculi în mod egal, s-a demonstrat că stimularea ganglionului stelat stâng crește dispersia repolarizării regionale în peretele anterior al ventriculului stâng și la apex, în timp ce stimularea ganglionului stelat drept influențează în principal peretele posterior al ventriculului drept.
Remodelarea Simpatică după Infarctul Miocardic
Leziunile cardiace, cum ar fi infarctul miocardic, duc la formarea cicatricilor, perturbă reglarea autonomă cardiacă și remodelează inervația simpatică. Infarctul cauzează denervare simpatică în interiorul cicatricii, rezultând un răspuns anormal la simpatoexcitație. Miocardul supraviețuitor demonstrează o scurtare heterogenă a perioadei refractare efective (ERP) indusă de stimularea ganglionului stelat și perfuzia de norepinefrină. Regenerarea nervoasă și hiperinervația simpatică pot fi aritmogene, contribuind la un risc mai mare de moarte subită cardiacă.
Implicații Clinice ale Modulării Simpatice
Dezechilibrul autonom, interacționând cu instabilitatea electrică a miocardului, a condus la dezvoltarea terapiilor neuromodulatoare, care vizează restabilirea acestui echilibru prin scăderea semnalizării eferente simpatice și/sau creșterea activității parasimpatice. Iată câteva intervenții actuale:
| Intervenție | Mecanism | Indicații | Note cheie |
|---|---|---|---|
| Anestezia Transepidurală (TEA) | Blocarea fibrelor simpatice T1-T4 și C8 | Aritmii ventriculare refractare (ES) | Potențial mai completă decât SGB, dar fără parametri fiabili de succes. |
| Denervarea Nervilor Renali (RND) | Ablația nervilor renali aferenți și eferenți, scade catecolaminele circulante | Hipertensiune rezistentă, AF cu HTN, aritmii ventriculare refractare | Re-inervație posibilă, distribuție heterogenă a nervilor renali. |
| Denervarea Simpatică Cardiacă (CSD) | Disrupe fibrele aferente și eferente prin îndepărtarea lanțului simpatic și a ganglionului stelat | Sindromul QT lung, tahicardie ventriculară polimorfă catecolaminergică, ES | Procedură invazivă, CSD bilateral mai eficient, complicații (sindrom Horner, hipotensiune). |
| Blocada Ganglionului Stelat (SGB) | Inhibiție farmacologică temporară a ganglionilor stelați cervicali | ES (terapie de salvare), durere | Procedură la pat, fără sedare, efect temporar, fără parametri clari de succes. |
| Stimularea Baroreceptorilor Carotidieni | Activează aferențele, stimulează eferențele parasimpatice, inhibă aferențele simpatice | Insuficiență cardiacă, hipertensiune (potențial și aritmii) | Eficacitatea antiaritmică la om încă nu este pe deplin demonstrată. |
| Stimularea Nervoasă Subcutanată (ScNS) | Stimularea electrică a nervilor simpatici subcutanați | Fibrilație atrială (în studiu) | Metodă nouă, necesită studii suplimentare. |
Direcții Viitoare în Modularea Simpatică
Cercetarea continuă să exploreze noi modalități de a modula activitatea simpatică pentru a combate aritmiile și a îmbunătăți sănătatea cardiovasculară:
- Modularea Farmacologică Simpatică: Beta-blocantele rămân un pilon, dar noi agenți precum Ivabradina (un blocant If) și antagoniștii receptorilor NPY Y1 (precum BIBO 3304) ar putea oferi opțiuni suplimentare. Neuropeptida Y (NPY), eliberată în timpul stimulării simpatice de nivel înalt, a apărut ca o țintă promițătoare, nivelurile ridicate fiind asociate cu rezultate mai proaste în insuficiența cardiacă și aritmii recurente.
- Ablația Ganglionului Aortorenal (ARG): Această tehnică vizează direct ganglionii aortorenali, care pot influența semnificativ hemodinamica. Studiile preliminare la animale sugerează că ablația ARG ar putea oferi un efect cardioprotector împotriva aritmiilor induse de ischemie, fiind mai eficientă decât ablația nervilor renali convenționali.
- Deaferentarea cu Resiniferatoxină (RTX): RTX este un activator puternic și ireversibil al canalului TRPV1, care mediază parțial membrul aferent al reflexului aferent simpatic cardiac (CSAR). Aplicarea epicardială a RTX în modelele animale de infarct a abolit CSAR, atenuând inducibilitatea aritmiilor ventriculare și progresia insuficienței cardiace.
- CSD Modificat: Abordări mai puțin invazive ale CSD, cum ar fi ablația cu radiofrecvență unipolară a lanțului simpatic proximal (T2-T5) cu cruțarea ganglionului stelat, sunt investigate pentru a reduce timpul procedurii și complicațiile, oferind totuși o reducere substanțială a aritmiilor ventriculare.
- Terapia de Modulare Axonală (AMT): Această terapie în curs de dezvoltare vizează controlul selectiv și la cerere al activității simpatice cardiace prin blocarea selectivă a potențialelor de acțiune axonale folosind curenți alternativi de înaltă frecvență (KHFAC) sau curenți direcți echilibrați.
- Stimularea Magnetică și cu Ultrasunete: Stimularea magnetică transcraniană și stimularea electromagnetică a trunchiurilor parasimpatice au fost investigate pentru impactul lor asupra ritmului cardiac și a variabilității ritmului cardiac. De asemenea, stimularea magnetică transcutanată și stimularea cu ultrasunete de nivel scăzut a ganglionului stelat stâng au demonstrat beneficii în suprimarea aritmiilor ventriculare în modele animale.
- Modularea Celulelor Gliale: Celulele gliale satelite, care învelesc neuronii și influențează activitatea sinaptică, sunt investigate pentru rolul lor în patofiziologia aritmiilor. Activarea celulelor gliale satelite ar putea modula output-ul simpatic și ar putea servi drept țintă terapeutică.
Întrebări Frecvente (FAQ)
Pentru a clarifica aspectele cheie ale reflexelor cardiovasculare și modulării simpatice, am compilat o serie de întrebări frecvente:
- Ce sunt reflexele cardiovasculare și de ce sunt importante?
Reflexele cardiovasculare sunt mecanisme neurale complexe care reglează rapid funcția inimii și a vaselor de sânge, adaptându-le la nevoile corpului. Ele sunt cruciale pentru menținerea tensiunii arteriale, a ritmului cardiac și a fluxului sanguin către organele vitale, asigurând homeostazia și răspunsul la stres, exerciții fizice sau schimbări de mediu. - Cum influențează exercițiile fizice inima prin aceste reflexe?
În timpul exercițiilor, inima este influențată de trei mecanisme principale: comanda centrală (semnale din creier care anticipează efortul), reflexul presor la exercițiu (feedback de la mușchii în lucru despre condițiile metabolice și mecanice) și baroreflexul arterial (care se resetează pentru a permite o tensiune arterială mai mare, dar o menține în limite sigure). Acestea lucrează împreună pentru a crește debitul cardiac și a redistribui fluxul sanguin către mușchii activi. - Poate stresul emoțional afecta ritmul cardiac prin reflexe?
Da, stresul emoțional, în special emoțiile puternice precum furia și frica, poate activa intens sistemul nervos simpatic, ducând la simpatoexcitație. Aceasta poate destabiliza electrofiziologia cardiacă, scurtând potențialul de acțiune și crescând eterogenitatea repolarizării, ceea ce predispune la aritmii ventriculare. - Ce este denervarea simpatică cardiacă (CSD) și când este utilizată?
CSD este o procedură chirurgicală minim invazivă sau video-asistată care implică întreruperea fibrelor nervoase simpatice care inervează inima, de obicei prin îndepărtarea lanțului simpatic și a ganglionilor stelați. Este utilizată ca terapie de ultimă instanță pentru aritmiile ventriculare refractare, în special la pacienții cu sindromul QT lung, tahicardie ventriculară polimorfă catecolaminergică sau furtună electrică. - Există modalități non-farmacologice de a îmbunătăți ritmul cardiac prin modularea reflexelor?
Da. Pe lângă exercițiile fizice (care trebuie adaptate individual), tehnici precum blocada ganglionului stelat (SGB) sau anestezia transepidurală (TEA) oferă o modulare temporară a activității simpatice. De asemenea, cercetările explorează stimularea baroreceptorilor carotidieni, stimularea nervoasă subcutanată și chiar stimularea magnetică sau cu ultrasunete a ganglionilor stelați ca metode non-farmacologice cu potențial antiaritmic.
Concluzie
Reglarea cardiovasculară este un domeniu de o complexitate remarcabilă, iar rolul interacțiunilor dintre sistemul nervos autonom și funcția cardiacă este din ce în ce mai bine înțeles. Reflexele cardiovasculare, precum reflexul trigemenocardiac, reflexul presor la exercițiu și baroreflexul arterial, sunt esențiale pentru adaptarea inimii la diverse condiții fiziologice și patologice. Simpatoexcitația joacă un rol crucial în modularea repolarizării ventriculare și în susceptibilitatea la aritmii, deschizând calea pentru terapiile neuromodulatoare. Deși intervențiile precum denervarea simpatică cardiacă și blocada ganglionului stelat au demonstrat deja beneficii semnificative, acest domeniu este încă la început. Studiile viitoare vor continua să elucideze mecanismele delicate de control neural și să rafineze abordările terapeutice, deschizând noi orizonturi pentru gestionarea aritmiilor complexe și îmbunătățirea sănătății cardiovasculare.
Dacă vrei să descoperi și alte articole similare cu Reflexe Cardiovasculare și Ritmul Inimii, poți vizita categoria Sănătate.