17/06/2023
Progresele remarcabile în depistarea precoce și tratamentul cancerului au condus la o creștere semnificativă a numărului de supraviețuitori. Această evoluție pozitivă a adus însă în prim-plan o nouă provocare medicală: impactul terapiilor oncologice asupra sănătății cardiovasculare. Domeniul emergent al cardio-oncologiei se concentrează pe intersecția complexă dintre bolile cardiovasculare și cancer, având ca scop principal asigurarea celui mai bun tratament oncologic, minimizând în același timp riscul de toxicitate cardiovasculară. În acest context, Societatea Europeană de Cardiologie (ESC) a publicat în 2022 primele sale ghiduri cuprinzătoare privind cardio-oncologia, marcând un moment crucial în îngrijirea pacienților cu cancer și a supraviețuitorilor.

- Ce Reprezintă Ghidurile ESC de Cardio-Oncologie 2022?
- Evaluarea Riscului Cardiovascular Inițial
- Când Este Recomandată o Trimitere la Cardio-Oncologie?
- Strategii de Prevenție a Toxicității Cardiovasculare Legate de Terapia Anticanceroasă (CTR-CVT)
- Managementul Toxicităților Cardiovasculare Specifice
- Disfuncția Cardiacă Legată de Antracicline (CTRCD)
- Disfuncția Cardiacă Legată de Terapii Anti-HER2
- Complicații Cardiovasculare Asociate cu Inhibitorii Punctelor de Control Imun (ICI)
- Terapii cu Celule T cu Receptor Antigen Chimeric (CAR-T) și Limfocite Infiltrante Tumorale (TIL)
- Boala Cardiovasculară Indușă de Transplantul de Celule Stem Hematopoietice (HSCT)
- Sindromul Takotsubo
- Boala Arterială Coronariană (BAC)
- Boala Valvulară Cardiacă
- Aritmii Cardiace
- Hipertensiunea Arterială
- Tromboză și Tromboembolism
- Alte Managementuri Acute
- Evaluarea la Finalul Terapiei și Urmărirea pe Termen Lung
- Populații Speciale
- Concluzie și Direcții Viitoare
Ce Reprezintă Ghidurile ESC de Cardio-Oncologie 2022?
Aceste ghiduri, elaborate în colaborare cu Societatea Europeană de Radioterapie Oncologică (ESTRO), Asociația Europeană de Hematologie (EHA) și Societatea Internațională de Cardio-Oncologie (IC-OS), reprezintă o resursă fundamentală pentru toți profesioniștii din domeniul sănătății implicați în îngrijirea pacienților oncologici. Obiectivul lor este de a oferi îndrumare clară privind definirea, diagnosticul, tratamentul și prevenția toxicității cardiovasculare legate de terapia anticanceroasă (CTR-CVT), precum și managementul bolilor cardiovasculare cauzate direct sau indirect de cancer. Deși domeniul cardio-oncologiei este relativ nou, iar dovezile din studiile clinice randomizate sunt încă limitate, majoritatea recomandărilor (aproximativ 76%) se bazează pe consensul experților, studii retrospective sau date din registre, având un nivel de evidență C. Doar un procent mic de recomandări (3%) beneficiază de un nivel de evidență A.
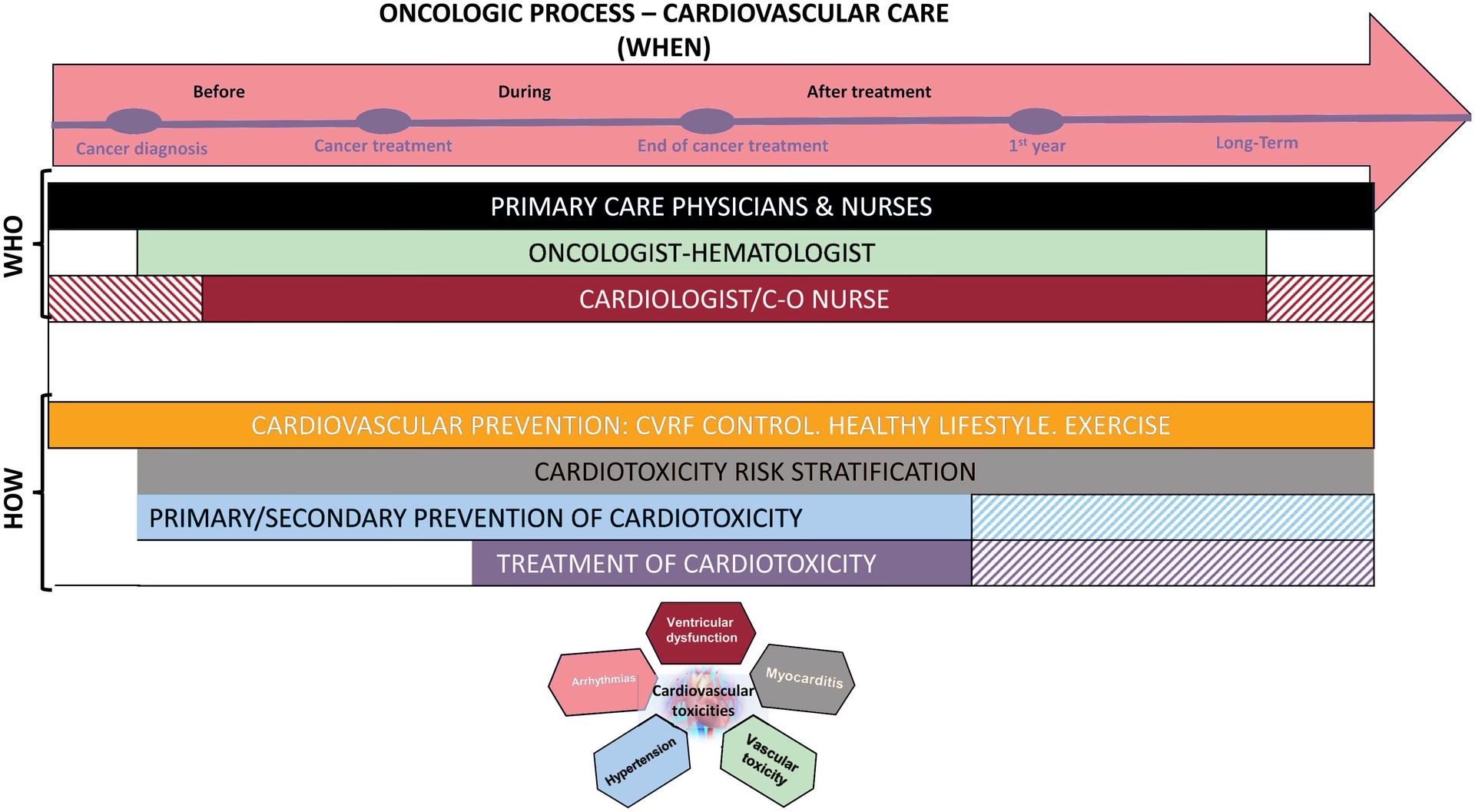
Ghidurile subliniază importanța unei abordări multidisciplinare pe tot parcursul parcursului terapeutic al pacientului, cu implicarea predominantă a cardiologilor, oncologilor și hematologilor. Deși o parte dintre pacienții cu cancer și afecțiuni cardiace pot fi gestionați conform ghidurilor ESC generale, mulți necesită o abordare specializată, iar aceste ghiduri completează o lacună crucială în cunoștințe.
Evaluarea Riscului Cardiovascular Inițial
Un aspect central al ghidurilor este evaluarea cuprinzătoare a riscului cardiovascular inițial, deoarece aceasta determină traiectoria viitoare a profilului de risc de CTR-CVT și tipul, intensitatea și durata supravegherii. Riscul de CTR-CVT este o variabilă dinamică, influențată de factori modificabili și nemodificabili, cum ar fi vârsta, sexul, genetica, istoricul de cancer și terapii anterioare, precum și factorii de risc cardiovascular preexistenți.
Ghidurile oferă o listă de verificare pentru evaluarea riscului de toxicitate cardiovasculară, care încorporează istoricul anterior de cancer și tratament, precum și istoricul cardiovascular și factorii de risc. Testele suplimentare recomandate la bază includ:
- Electrocardiograma (ECG) la toți pacienții.
- Ecocardiografia transtoracică (TTE) la pacienții cu risc înalt sau foarte înalt de CTR-CVT.
- Măsurarea biomarkerilor cardiaci (peptide natriuretice [NP] – BNP sau NT-proBNP, și troponina cardiacă [cTn]) dacă acești markeri vor fi utilizați pentru a evalua modificările dinamice în timpul urmăririi.
- Alte teste recomandate la bază: profil lipidic, glicemie à jeun sau HbA1c, și evaluarea funcției renale.
Pentru a evalua riscul de toxicitate cardiovasculară, ghidurile sugerează utilizarea scorului HFA-ICOS (Heart Failure Association-International Cardio-Oncology Society), un instrument complex care ia în considerare multiple variabile, de la boli cardiovasculare preexistente și imagistică, la biomarkeri, vârstă, comorbidități generale, tratament anterior al cancerului și factori legați de stilul de viață. Variabilele au ponderi diferite în funcție de tratamentul oncologic propus. Iată o versiune simplificată a factorilor de risc și a categoriilor asociate pentru anumite terapii:
| Factor de Risc Cardiovascular Inițial | Terapie cu Antracicline | Terapii Țintite HER2 |
|---|---|---|
| Insuficiență Cardiacă/Cardiomiopatie Preexistentă | Risc Foarte Ridicat (VH) | Risc Foarte Ridicat (VH) |
| Boală Valvulară Severă | Risc Ridicat (H) | Risc Ridicat (H) |
| Fibrilație Atrială/Alte Aritmii | Risc Moderat (M2) | Risc Moderat (M2) |
| Vârsta ≥ 80 ani | Risc Ridicat (H) | Risc Ridicat (H) |
| Hipertensiune Arterială | Risc Moderat (M1) | Risc Moderat (M1) |
| Diabet Zaharat | Risc Moderat (M1) | Risc Moderat (M1) |
| Expunere Anterioară la Antracicline | Risc Ridicat (H) | Risc Moderat (M2) |
| Radioterapie la Toracele Stâng/Mediastin | Risc Ridicat (H) | Risc Moderat (M2) |
Notă: VH = Risc Foarte Ridicat, H = Risc Ridicat, M2 = Risc Moderat (2 puncte), M1 = Risc Moderat (1 punct). Evaluarea completă implică un sistem de punctaj detaliat.
Când Este Recomandată o Trimitere la Cardio-Oncologie?
După finalizarea evaluării riscului de toxicitate cardiovasculară, pacienții sunt stratificați în diferite categorii de risc: scăzut, moderat, înalt și foarte înalt. Această stratificare ghidează deciziile privind necesitatea unei consultații cardiologice specializate:
- Pacienții cu risc înalt și foarte înalt de CTR-CVT beneficiază de o trimitere la cardiolog înainte de începerea tratamentului pentru cancer (Clasa I, Nivel de Evidență C).
- De asemenea, pacienților cu rezultate anormale la evaluarea inițială a riscului CV (ECG, biomarkeri cardiaci sau imagistică cardiacă) li se recomandă o trimitere la cardiolog (Clasa I, Nivel de Evidență C).
- În cazul pacienților cu risc moderat, o trimitere la cardio-oncologie poate fi luată în considerare în cazuri selecționate (Clasa IIb, Nivel de Evidență C).
- Pacienții cu risc scăzut pot începe terapia anticanceroasă fără întârziere (Clasa I, Nivel de Evidență C).
Aceste recomandări subliniază importanța intervenției timpurii pentru a minimiza riscurile cardiovasculare.
Strategii de Prevenție a Toxicității Cardiovasculare Legate de Terapia Anticanceroasă (CTR-CVT)
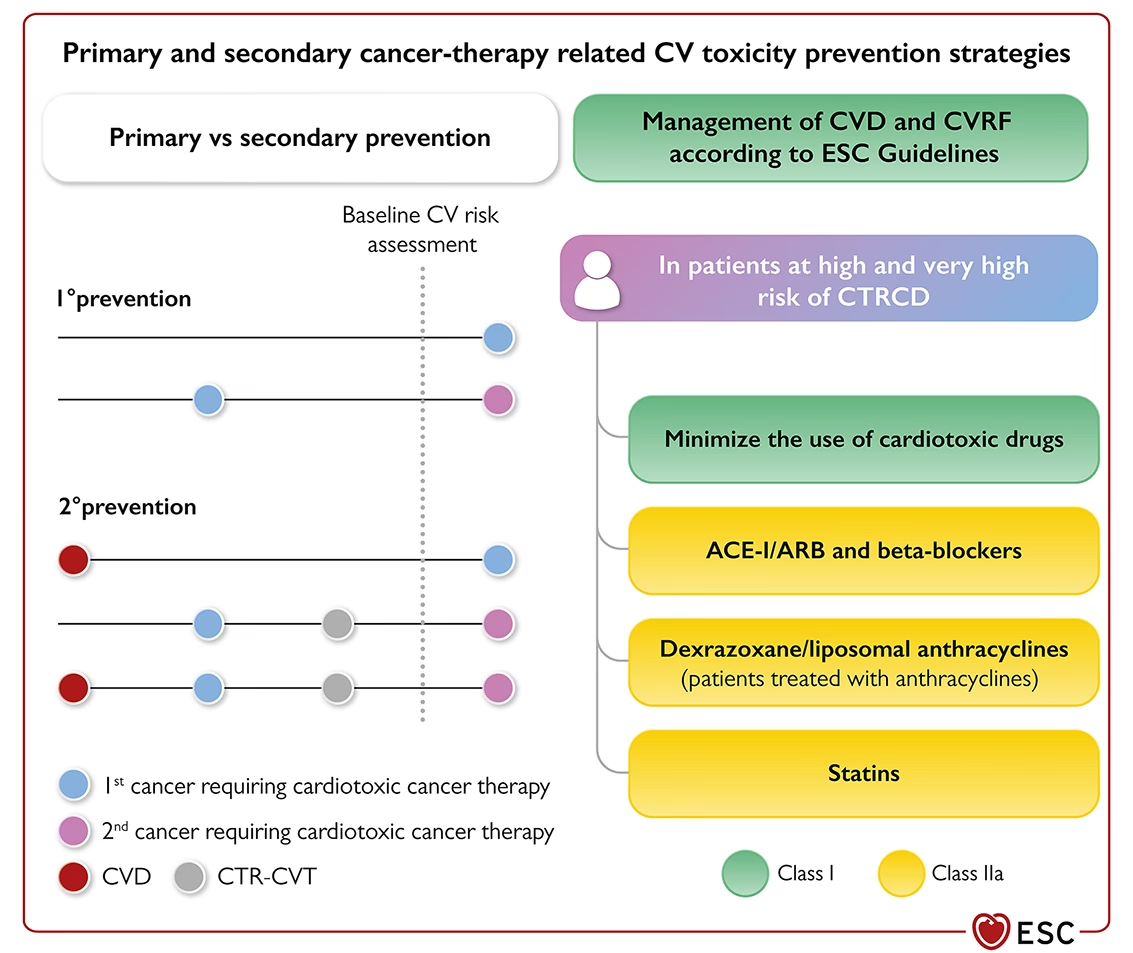
Prevenția CTR-CVT este esențială pentru a permite pacienților să primească cea mai bună terapie oncologică posibilă. Ghidurile ESC oferă recomandări specifice pentru pacienții cu risc înalt și foarte înalt de toxicitate cardiovasculară cu anumite tratamente:
- Antracicline: Pentru pacienții cu risc înalt și foarte înalt de CTR-CVT, se recomandă utilizarea antraciclinelor lipozomale. De asemenea, dexrazoxanul ar trebui luat în considerare la pacienții adulți care urmează să primească o doză cumulativă mare de antracicline pentru tratament curativ, precum și la cei cu risc înalt și foarte înalt de disfuncție cardiacă legată de terapia anticanceroasă (CTRCD), inclusiv cei cu insuficiență cardiacă preexistentă sau fracție de ejecție a ventriculului stâng (FEVS) redusă/normal-mică, atunci când terapia cu antracicline este considerată esențială (Clasa IIa, Nivel de Evidență B).
- Terapii Neurohormonale: Inhibitorii enzimei de conversie a angiotensinei (IECA) sau blocanții receptorilor de angiotensină (BRA), beta-blocantele și statinele ar trebui luate în considerare la pacienții care primesc antracicline și/sau terapii țintite HER2, precum și la cei care primesc alte terapii anticanceroase asociate cu insuficiența cardiacă, dacă sunt la risc înalt sau foarte înalt de CTR-CVT (Clasa IIa, Nivel de Evidență B/C).
- Statine: Statinele sunt recomandate pentru prevenția primară la pacienții cu cancer cu risc înalt și foarte înalt de CTR-CVT (Clasa IIa, Nivel de Evidență B).
- Modificări ale stilului de viață: Adoptarea unui stil de viață sănătos, incluzând exercițiul fizic regulat și o nutriție adecvată, este crucială. Deși exercițiile fizice sunt benefice pentru condiția cardiorespiratorie, ghidurile menționează că nu există un beneficiu clar al exercițiilor efectuate înainte sau în timpul tratamentului pentru cancer pentru a reduce CTRCD. Cu toate acestea, ele fac parte dintr-o abordare integrată de prevenție.
Managementul Toxicităților Cardiovasculare Specifice
Ghidurile abordează o gamă largă de toxicități cardiovasculare specifice, oferind recomandări detaliate pentru fiecare, cu accent pe managementul multidisciplinar:
Disfuncția Cardiacă Legată de Antracicline (CTRCD)
Managementul este stratificat în funcție de prezența sau absența simptomelor. Pentru pacienții simptomatici, terapia pentru insuficiență cardiacă trebuie inițiată conform ghidurilor standard ESC, iar decizia de a continua sau întrerupe antraciclinele depinde de severitatea simptomelor. La pacienții asimptomatici cu CTRCD moderată sau severă, tratamentul ar trebui întrerupt, în timp ce cei cu boală ușoară pot continua tratamentul, cu introducerea IECA/BRA și/sau beta-blocantelor dacă sunt îndeplinite anumite criterii. Antraciclinele lipozomale și dexrazoxanul pot fi utilizate ca strategii de prevenție secundară dacă antraciclinele sunt reluate după apariția CTRCD moderate sau severe.
Disfuncția Cardiacă Legată de Terapii Anti-HER2
Abordarea este mai permisivă în ceea ce privește continuarea terapiei, reflectând o probabilitate mai mare de recuperare a funcției ventriculare stângi. Pacienții simptomatici cu CTRCD moderată până la severă ar trebui să întrerupă tratamentul anti-HER2 și să înceapă terapia pentru insuficiență cardiacă. Decizia de a relua sau opri tratamentul anti-HER2 ar trebui luată de o echipă multidisciplinară (MDT). Pentru pacienții asimptomatici, cei cu boală moderată și ușoară pot continua tratamentul anti-HER2 cu monitorizare crescută (TTE, cTn și NP) și luarea în considerare a IECA/BRA și beta-blocantelor.
Complicații Cardiovasculare Asociate cu Inhibitorii Punctelor de Control Imun (ICI)
Inhibitorii punctelor de control imun sunt asociați cu o serie de toxicități CV directe (miocardită, aritmii, sindrom coronarian acut, accident vascular cerebral, inflamație pericardică, dislipidemie, sindrom Takotsubo) și indirecte (inflamația glandelor tiroidă, suprarenală și hipofiză, precum și modificări vasculare ducând la un risc crescut de tromboză arterială și venoasă). Miocardita asociată cu ICI, deși rară, are o rată de mortalitate ridicată. Diagnosticul ar trebui suspectat la pacienții cu simptome CV sau evenimente adverse non-cardiace legate de imunitate (în special miastenie, miozită și miopatie) asociate cu o elevare a troponinei și modificări noi la ECG. Metilprednisolonul intravenos ar trebui inițiat prompt la pacienții hemodinamic instabili, iar terapia ICI ar trebui întreruptă. Imagistica cardiacă urgentă (TTE, RMN cardiacă) este necesară. Orice decizie de a reîncepe ICI după recuperare ar trebui discutată în cadrul unei MDT.
Terapii cu Celule T cu Receptor Antigen Chimeric (CAR-T) și Limfocite Infiltrante Tumorale (TIL)
Recomandările pentru managementul CTRCD în cazul terapiilor CAR-T și TIL derivă din studii mai mici și rapoarte de caz. Cele mai multe evenimente adverse cu terapia CAR-T sunt legate de sindromul de eliberare a citokinelor (CRS), care poate duce la aritmii, insuficiență cardiacă, infarct miocardic și tromboembolism venos. Pacienții necesită monitorizare ECG, TTE, evaluarea cTn și NP, și îngrijire de nivel 3. Complicațiile cardiace cu TIL, deși comune, nu par să afecteze supraviețuirea, iar ghidul nu are recomandări specifice pentru managementul CV dincolo de îndrumările standard ESC.
Boala Cardiovasculară Indușă de Transplantul de Celule Stem Hematopoietice (HSCT)
O gamă largă de complicații CV pot apărea în timpul HSCT. Există o lipsă relativă de dovezi pentru intervențiile care limitează toxicitatea CV în această cohortă, iar ghidurile solicită studii suplimentare în acest domeniu, inclusiv rolul exercițiilor fizice înainte și după transplant.
Sindromul Takotsubo
Numeroși factori etiologici sunt responsabili pentru sindromul Takotsubo (TTS) la pacienții cu cancer, inclusiv tratamentele administrate și stresul emoțional asociat cu diagnosticul. Ghidul recomandă angiografie cu CT sau angiografie coronariană invazivă, alături de RMN cardiacă pentru a căuta dovezi de infarct sau miocardită. Dacă se suspectează o medicație cauzatoare, aceasta ar trebui oprită în faza acută, iar decizia de a o reîncepe ar trebui luată de o MDT.
Boala Arterială Coronariană (BAC)
Pacienții cu cancer prezintă un risc crescut de sindrom coronarian acut (SCA) comparativ cu populația generală. Pe lângă ruptura plăcii aterosclerotice, vasospasmul (indus de fluoropirimidine) și tromboza coronariană sunt etiologii prevalente. Ghidurile evidențiază că pacienții cu cancer beneficiază mai puțin frecvent de management invaziv coronarian, dar unde este utilizată, intervenția coronariană percutanată (PCI) este asociată cu o reducere a evenimentelor adverse și a mortalității. O strategie invazivă precoce este recomandată pentru pacienții cu cancer și STEMI sau NSTEMI cu risc înalt, cu o speranță de viață mai mare de 6 luni. Pentru pacienții cu trombocitopenie, există recomandări specifice privind pragurile de număr de trombocite pentru PCI și CABG, precum și pentru utilizarea agenților antiplachetari.
Boala Valvulară Cardiacă
Ghidurile abordează două situații principale: pacienții cu boală valvulară severă preexistentă și cei care dezvoltă o boală valvulară severă în timpul terapiei pentru cancer. În ambele situații, pacienții ar trebui gestionați în conformitate cu ghidurile ESC/EACTS, iar o MDT este necesară pentru a determina tipul optim de tratament valvular, luând în considerare prognosticul cancerului, fezabilitatea tehnică a intervenției chirurgicale, urgența tratamentului oncologic și prezența comorbidităților.
Aritmii Cardiace
Ghidurile abordează managementul fibrilației atriale (FA), al aritmiilor ventriculare, al intervalelor QT corectate lungi și al bradiaritmiilor. Decizia de anticoagulare în FA utilizează modelul TBIP (risc tromboembolic, risc de sângerare, interacțiuni medicamentoase, preferințele pacientului și disponibilitatea medicamentului). Scorurile precum CHA2DS2-VASc sunt folosite, dar se iau în considerare și factori specifici cancerului pentru riscul de sângerare (trombocitopenie, tumori gastro-intestinale/genito-urinare, sângerări active/recente). Anticoagulantele orale directe (DOAC) sunt preferate în majoritatea cazurilor, cu heparina cu greutate moleculară mică (LMWH) ca a doua opțiune.
Majoritatea aritmiilor ventriculare sunt legate de prelungirea intervalului QTc, ducând la torsada vârfurilor (TdP). Ghidurile recomandă oprirea medicamentului cauzator dacă QTc ≥ 500 ms și corectarea factorilor reversibili. Pentru bradiaritmii, în contextul bolii de conducere AV induse de ICI, se recomandă monitorizare ECG serială și metilprednisolon IV.
Hipertensiunea Arterială
Obiectivul tratamentului hipertensiunii este de a preveni întreruperile inutile ale terapiei pentru cancer și de a reduce complicațiile cardiovasculare. Recomandările privind pragul de tratament iau în considerare prognosticul cancerului, cu ținte mai puțin stricte pentru pacienții cu cancer metastatic și speranță de viață redusă. IECA/BRA sunt agenți de primă linie, iar blocantele canalelor de calciu dihidropiridinice (CCB) sunt de linia a doua. CCB non-dihidropiridinice ar trebui evitate din cauza potențialului de interacțiuni medicamentoase.
Tromboză și Tromboembolism
Tromboembolismul venos (TEV) este semnificativ mai comun la pacienții cu cancer. Atât DOAC-urile (apixaban, edoxaban sau rivaroxaban), cât și LMWH au recomandări de nivel IA pentru tratamentul TEV la pacienții care primesc tratament pentru cancer. Pentru prevenția primară, pacienții spitalizați sau cei cu repaus prelungit la pat ar trebui să primească LMWH profilactic.
Alte Managementuri Acute
- Boala Arterială Periferică (BAP): Managementul urmează ghidurile standard, dar cu o atenție sporită la interacțiunile medicamentoase și riscul de sângerare.
- Hipertensiunea Pulmonară (HP): Dasatinib este puternic asociat cu HP. Ghidurile recomandă întreruperea acestuia dacă viteza regurgitării tricuspidiene (TRV) este > 3,4 m/s.
- Boli Pericardice: Managementul pericarditei urmează, în general, îndrumările stabilite de ESC. În cazurile asociate cu ICI, dacă efuziunea este moderată până la severă, ICI ar trebui întrerupt, iar colchicina și prednisolonul ar trebui utilizate pentru a reduce inflamația.
Evaluarea la Finalul Terapiei și Urmărirea pe Termen Lung
Ghidurile separă evaluarea riscului în primele 12 luni după tratament de evaluarea continuă a riscului și supravegherea după această perioadă inițială, incluzând atât supraviețuitorii adulți, cât și pe cei din copilărie și adolescență. Aceste recomandări sunt relevante doar pentru pacienții cu un prognostic bun pe termen lung. Pacienții sunt stratificați în grupuri de risc foarte înalt, înalt, moderat și scăzut, atât în funcție de riscul precoce, cât și de cel tardiv, și de simptomatologie.
Terapii asociate cu risc pe termen lung de complicații CV includ doze de doxorubicină ≥ 250 mg/m2, radioterapie cu o doză medie cardiacă (MHD) > 15 Gy, doxorubicină ≥ 100 mg/m2 combinată cu radioterapie 5–15 Gy MHD, și receptori de transplant de celule stem hematopoietice cu risc înalt. Educarea pacienților cu privire la alegerile sănătoase de stil de viață, riscul lor de boală și simptomele CV cardinale de urmărit este recomandată; acest lucru este deosebit de important la supraviețuitorii din copilărie și adolescență ai terapiilor pentru cancer, unde CTRCD este un contributor semnificativ la morbiditate și mortalitate mai târziu în viață. De la 12 luni, se recomandă screening anual și monitorizare a factorilor de risc CV modificabili. Pacienții adulți ar trebui să aibă o restratificare a riscului la 5 ani post-terapie, iar toți pacienții cu simptome cardiovasculare emergente ar trebui să aibă o evaluare cardiologică.
În ceea ce privește imagistica, supraviețuitorii adulți cu risc moderat ar trebui să facă un TTE la fiecare 5 ani, iar cei cu risc înalt sau foarte înalt ar trebui să facă un TTE la 1, 3 și 5 ani după terapie. Supraviețuitorii din copilărie și adolescență ar trebui să facă un TTE la fiecare 5 ani dacă sunt la risc moderat și la fiecare 2 ani dacă sunt la risc înalt sau foarte înalt.
Populații Speciale
Secțiunea finală a ghidurilor acoperă o serie de populații speciale și condiții rare, dar importante, care necesită o abordare particularizată în cardio-oncologie. Aceasta include tumori cardiace primare, evaluarea cardiacă a pacienților gravide cu cancer, boala cardiacă carcinoidă, amiloidoza cardiacă cu lanțuri ușoare de amiloid și interacțiunile dintre radioterapie și funcția dispozitivelor cardiace implantabile electronice (CIED), cum ar fi stimulatoarele cardiace și defibrilatoarele.
Concluzie și Direcții Viitoare
Noile ghiduri ESC de cardio-oncologie oferă o piatră de temelie pentru recomandările adresate cardiologilor specialiști și generaliști care tratează pacienți cu cancer și reprezintă o realizare remarcabilă, având în vedere amploarea și profunzimea documentului într-un domeniu relativ nou. Există, totuși, numeroase aspecte care trebuie abordate în viitor pentru a asigura că multe dintre recomandări au o bază de dovezi mai solidă. Autorii recunosc acest lucru și stabilesc multe direcții viitoare pentru formare, furnizarea de servicii și cercetare, inclusiv necesitatea unor căi de formare care să cuprindă o abordare multidisciplinară, studii pentru a valida instrumentele de evaluare a riscului HFA-ICOS și evaluarea impactului susceptibilității genetice la cardiotoxicitate cu anumite tratamente pentru cancer.
Din perspectivă practică, este necesară o mai bună înțelegere a impactului cardiovascular al combinațiilor de tratamente (dincolo de antracicline și radioterapie), definirea cost-eficienței strategiilor de screening și supraveghere și impactul acestora asupra rezultatelor pe termen lung la pacienții cu cancer, și stabilirea modului în care această abordare intensivă în resurse va fi implementată practic în sistemele de sănătate. Prin conturarea „necunoscutelor cunoscute” în secțiunile finale ale documentului, a fost stabilită o foaie de parcurs pentru viitorul cardio-oncologiei, oferind un teren fertil pentru extinderea subspecialității.
Întrebări Frecvente (FAQ)
1. Ce este cardio-oncologia?
Cardio-oncologia este o specialitate medicală emergentă care se ocupă cu prevenția, diagnosticul și tratamentul problemelor cardiovasculare care apar la pacienții cu cancer, fie ca efect secundar al terapiilor anticanceroase, fie ca o consecință directă a bolii în sine.
2. De ce sunt importante Ghidurile ESC de Cardio-Oncologie 2022?
Aceste ghiduri sunt primele de acest fel publicate de Societatea Europeană de Cardiologie și oferă o abordare structurată și bazată pe dovezi (sau consens de experți, unde dovezile sunt limitate) pentru gestionarea sănătății cardiovasculare a pacienților cu cancer, de la evaluarea riscului inițial până la supravegherea pe termen lung.
3. Cum îmi pot reduce riscul cardiovascular în timpul tratamentului pentru cancer?
Reducerea riscului implică o evaluare atentă înainte de tratament, utilizarea agenților cardioprotectori (cum ar fi dexrazoxanul sau anumite medicamente cardiovasculare) dacă sunteți la risc înalt, și adoptarea unui stil de viață sănătos (dietă echilibrată, exerciții fizice moderate, evitarea fumatului). Medicul dumneavoastră va personaliza strategia de prevenție.
4. Când ar trebui să văd un cardiolog dacă am cancer?
O trimitere la cardiolog este recomandată dacă sunteți considerat la risc înalt sau foarte înalt de toxicitate cardiovasculară înainte de începerea tratamentului oncologic, sau dacă aveți rezultate anormale la testele cardiace inițiale (ECG, ecocardiografie, biomarkeri). De asemenea, orice apariție a simptomelor cardiovasculare noi în timpul sau după tratament necesită o evaluare cardiologică.
5. Ce se întâmplă după terminarea tratamentului pentru cancer?
Supravegherea cardiovasculară continuă și după încheierea tratamentului oncologic, mai ales la pacienții cu un prognostic bun pe termen lung. Aceasta include screening anual, gestionarea factorilor de risc cardiovascular modificabili și, în funcție de nivelul de risc, monitorizare imagistică cardiacă periodică (ecocardiografii). Educația privind un stil de viață sănătos rămâne vitală.
Dacă vrei să descoperi și alte articole similare cu Ghidul ESC de Cardio-Oncologie: Inima și Cancerul, poți vizita categoria Fitness.