19/12/2025
Inima, un organ vital, este adesea supusă unui stres constant, iar în fața acestor provocări, dezvoltă mecanisme complexe de adaptare. Unul dintre cele mai puțin înțelese, dar din ce în ce mai studiate, este rolul proteinei EPAC (Exchange Protein Directly Activated by cAMP). Deși efectele sale sunt mult mai puțin cunoscute decât cele ale efectorului clasic al cAMP, PKA (Protein Kinase A), numeroase studii au investigat rolul cardiac al EPAC, oferind dovezi că EPAC modulează semnificativ homeostazia calciului intracelular și influențează procese cheie precum hipertrofia cardiacă și, crucial, fibroza cardiacă. Acest articol explorează în profunzime modul în care EPAC afectează dezvoltarea fibrozei cardiace și de ce este considerat un regulator emergent și o potențială țintă terapeutică în patofiziologia cardiovasculară.
Ce Este EPAC și Cum Funcționează?
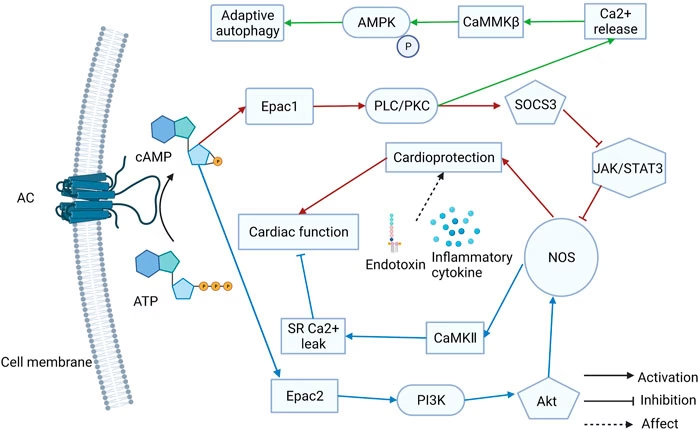
EPAC, sau "Exchange Protein Directly Activated by cAMP", reprezintă o familie de proteine care, spre deosebire de PKA, sunt activate direct de AMP ciclic (cAMP) și acționează ca factori de schimb de nucleotide guanină (GEF) pentru proteinele Ras, în special Rap1. Această activare directă de către cAMP plasează EPAC într-o poziție cheie în cascada de semnalizare a AMP ciclic, oferind o cale alternativă la binecunoscuta cale PKA. Există două izoforme principale, EPAC1 și EPAC2, care diferă prin distribuția lor tisulară și, într-o oarecare măsură, prin rolurile lor funcționale.
Mecanismul de acțiune al EPAC este complex și implică mai multe etape. Atunci când nivelurile de cAMP cresc în celulă, cAMP se leagă direct de domeniile de legare ale cAMP (CBD) ale EPAC. Această legare induce o modificare conformațională în structura EPAC, expunând domeniul său catalitic GEF. Odată activat, EPAC facilitează schimbul de GDP cu GTP pe proteinele Rap1, transformând astfel Rap1 dintr-o stare inactivă (legată de GDP) într-o stare activă (legată de GTP). Rap1-GTP activat, la rândul său, poate interacționa cu o serie de efectori din aval, declanșând diverse răspunsuri celulare.
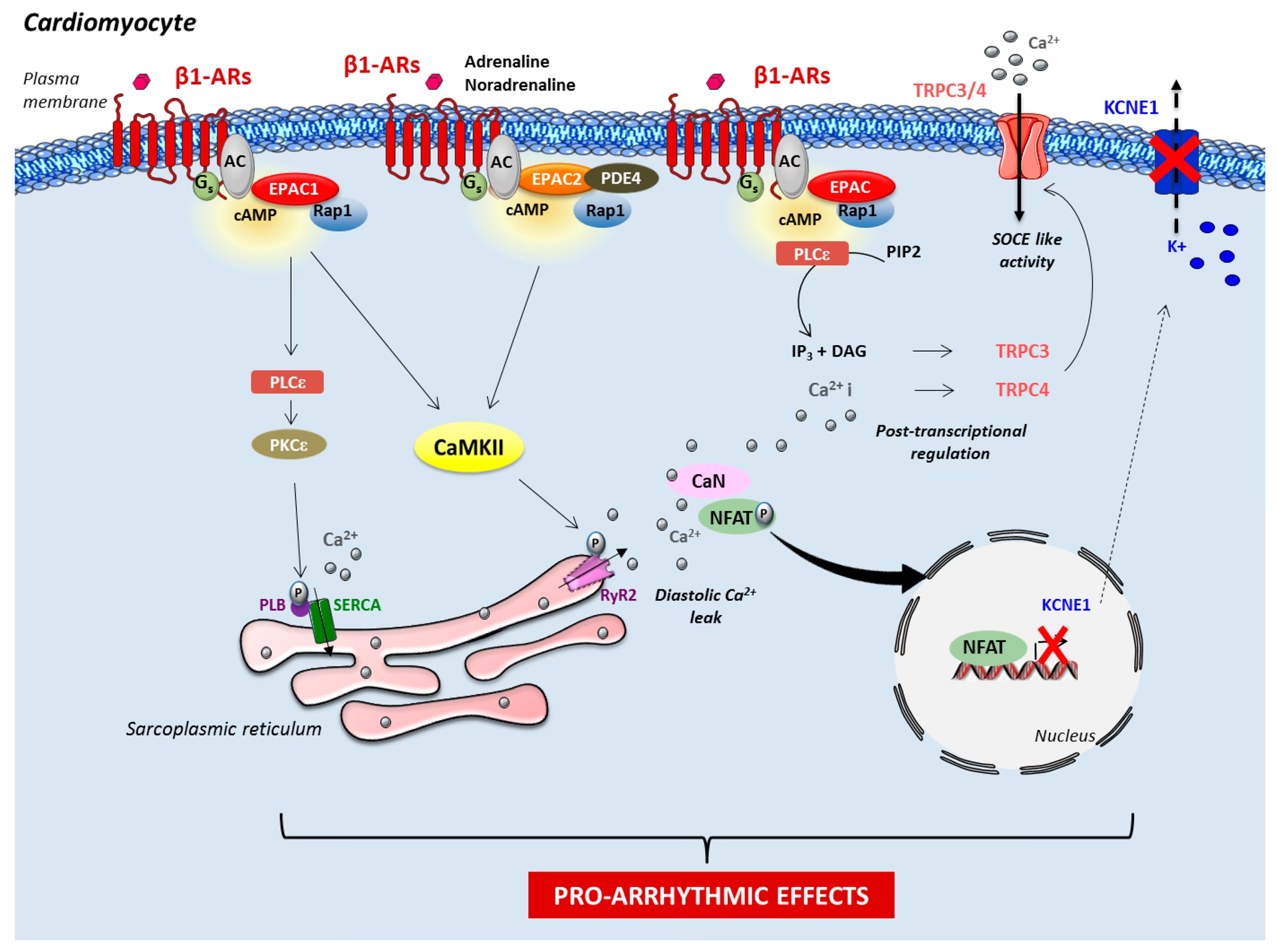
În inimă, una dintre primele analize a arătat că EPAC poate crește frecvența oscilațiilor spontane de calciu (Ca2+) în cardiomiocitele cultivate. Ulterior, în cardiomiocitele adulte, s-a demonstrat că EPAC poate induce eliberarea de Ca2+ din reticulul sarcoplasmatic (RS) într-un mod independent de PKA. Această cale implică fosfolipaza C (PLC) și kinaza Ca2+/calmodulină II (CaMKII). CaMKII, la rândul său, fosforilează receptorul rianodinei (RyR), o componentă crucială a cuplării excitație-contracție (EC), crescând probabilitatea de apariție a scânteilor de Ca2+. Astfel, EPAC joacă un rol important în cuplarea excitație-contracție, un proces fundamental pentru funcția cardiacă. Mai mult, prin inducerea fosforilării RyR, EPAC poate fi aritmogen, contribuind la instabilitatea electrică a inimii.
O analiză detaliată a mobilizării Ca2+ în diferite microdomenii celulare a arătat că EPAC ridică preferențial Ca2+ în nucleoplasmă ([Ca2+]n). Acest efect, pe lângă PLC și CaMKII, a necesitat activarea receptorului inositol 1,4,5-trifosfat (IP3R). IP3R este un alt canal de eliberare a Ca2+, localizat predominant în zona perinucleară a miocitelor ventriculare adulte, unde s-a demonstrat că participă la cuplarea excitație-transcripție – procesul prin care Ca2+ activează transcripția genică. Dacă activarea EPAC este menținută pentru o anumită perioadă, se produce translocarea histon-deacetilazei (HDAC) în afara nucleului, ceea ce duce la de-represia factorului de transcripție MEF2 (myocyte enhancer factor). Aceste dovezi subliniază rolul EPAC în activarea cuplării excitație-transcripție. De fapt, s-a demonstrat că EPAC induce hipertrofia cardiomiocitelor. Acțiunile EPAC sunt rapide, dar dependente de timp și microdomeniu în miocitul cardiac, indicând un rol important în răspunsul cardiac la stres.

EPAC și Fibroza Cardiacă: O Relație Complexă
Fibroza cardiacă este un proces patologic caracterizat prin acumularea excesivă de matrice extracelulară, în special colagen, în țesutul cardiac. Aceasta duce la rigidizarea inimii, disfuncție diastolică și sistolică, și, în cele din urmă, la insuficiență cardiacă. Fibroblastele cardiace sunt celulele cheie responsabile de sinteza colagenului și de remodelarea matricei extracelulare. În contextul patologiilor cardiace, aceste fibroblaste pot deveni activate, transformându-se în miofibroblaste, care contribuie activ la procesul de fibroză.
Datele actuale sugerează că EPAC este un integrator al semnalelor pro- și anti-fibrotice, având un rol nuanțat în dezvoltarea fibrozei cardiace. Un studiu important a arătat că EPAC este implicat în reglarea sintezei de colagen de către fibroblastele cardiace, mediată de adenozină. Această descoperire sugerează o legătură directă între activarea EPAC și producția de colagen, un aspect fundamental al fibrozei. În plus, s-a observat că receptorii beta-adrenergici stimulează producția de interleukină-6 (IL-6) – o citokină pro-inflamatorie cunoscută pentru rolul său în promovarea fibrozei – prin activarea dependentă de EPAC a căii de semnalizare PKCdelta/p38 MAPK în fibroblastele cardiace neonatale de șoarece. Aceasta indică un mecanism prin care EPAC poate contribui la un mediu pro-fibrotic în inimă.
Pe lângă implicarea directă în sinteza colagenului și producția de IL-6, rolul EPAC în hipertrofia cardiacă este, de asemenea, relevant pentru fibroză. Hipertrofia, o creștere a dimensiunii cardiomiocitelor ca răspuns la stres, este adesea un precursor al fibrozei și al insuficienței cardiace. Deoarece EPAC induce hipertrofia cardiomiocitelor, este plauzibil ca activarea cronică a EPAC să contribuie indirect la fibroză prin promovarea remodelării structurale generale a inimii. Răspunsul cardiac la stres, în care EPAC are un rol important, include nu doar adaptări contractile, ci și modificări structurale profunde care pot duce la fibroză.
Un alt aspect de luat în considerare este interacțiunea EPAC cu alte căi de semnalizare care reglează remodolarea cardiacă. De exemplu, fosfodiesteraza 1A (PDE1A), o enzimă care degradează cAMP, a fost identificată ca un regulator cheie al activării fibroblastelor cardiace și al remodelării matricei extracelulare. Deși nu este direct EPAC, modularea nivelurilor de cAMP poate influența activitatea EPAC și, prin urmare, indirect, și fibroza. Complexitatea semnalizării cAMP și interacțiunile dintre PKA și EPAC subliniază necesitatea unei înțelegeri mai profunde a modului în care aceste căi colaborează sau se opun în contextul bolilor cardiace.
Iată o scurtă sinteză a rolurilor EPAC în contextul patologiei cardiace:
| Aspect | Rolul EPAC | Implicare în Boala Cardiacă |
|---|---|---|
| Homeostazia Calciului | Creșterea oscilațiilor Ca2+, eliberarea Ca2+ din RS via PLC/CaMKII/RyR, creșterea Ca2+ nucleoplasmatic via IP3R. | Disfuncție contractuală, aritmogeneză. |
| Cuplarea Excitație-Contracție | Modularea funcției RyR și a eliberării Ca2+. | Impact direct asupra forței de contracție și relaxare. |
| Cuplarea Excitație-Transcripție | Translocarea HDAC, de-represia MEF2. | Inducerea hipertrofiei cardiace. |
| Hipertrofia Cardiacă | Induce creșterea dimensiunii cardiomiocitelor. | Factor de risc pentru insuficiență cardiacă și fibroză. |
| Fibroza Cardiacă | Integrează semnale pro- și anti-fibrotice; reglează sinteza colagenului și producția de IL-6 în fibroblaste. | Contribuie la rigidizarea și disfuncția cardiacă. |
| Aritmii | Fosforilarea RyR, modificarea curenților ionici (ex: IK, ICa, INa tardiv). | Creșterea riscului de aritmii fatale. |
EPAC: O Nouă Țintă Terapeutică pentru Bolile Cardiovasculare?
Având în vedere rolurile sale diverse și profunde în fiziologia și patofiziologia cardiacă, EPAC a început să fie recunoscut ca o țintă terapeutică atractivă pentru tratamentul diferitelor tulburări cardiovasculare. Înțelegerea mecanismelor specifice prin care EPAC contribuie la progresia bolii oferă noi perspective pentru dezvoltarea de medicamente inovatoare.
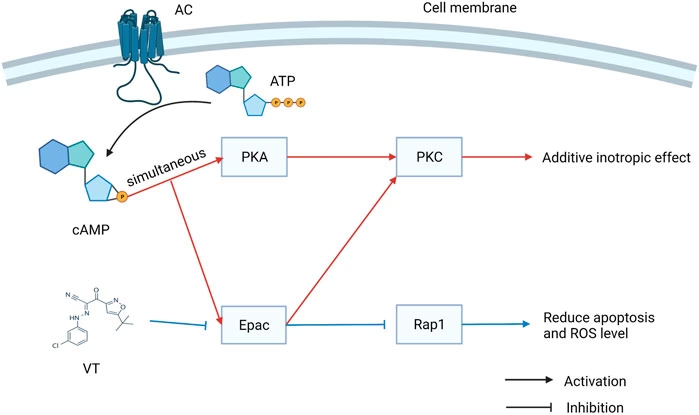
De exemplu, în contextul fibrozei, modularea activității EPAC ar putea reprezenta o strategie eficientă. Dacă EPAC integrează semnale pro- și anti-fibrotice, atunci manipularea sa farmacologică ar putea înclina balanța către un răspuns anti-fibrotic. Inhibitori specifici ai EPAC sau, dimpotrivă, agoniști, ar putea fi dezvoltați pentru a viza aspecte specifice ale remodelării cardiace. Există deja analogi specifici de cAMP pentru EPAC, precum 8-pCPT-2′-O-Me-cAMP-AM, și, de asemenea, inhibitori precum ESI-09, care au fost folosiți în studii experimentale pentru a investiga funcțiile EPAC. Aceste instrumente farmacologice permit o explorare mai detaliată a rolului EPAC în condiții de boală și deschid calea pentru viitoare terapii.
Mai mult, având în vedere implicarea EPAC în hipertrofia cardiacă și în aritmii, țintirea EPAC ar putea oferi beneficii multiple. Un compus care ar putea atenua hipertrofia indusă de EPAC, fără a afecta negativ funcția contractilă normală, ar fi de mare valoare. De asemenea, modularea EPAC pentru a reduce aritmogenitatea ar putea fi crucială în tratamentul unor afecțiuni precum fibrilația atrială sau aritmiile ventriculare. Cercetările actuale se concentrează pe dezvoltarea de molecule mici care să activeze sau să inhibe selectiv izoformele EPAC1 și EPAC2, având în vedere diferențele subtile în localizarea și funcția lor.
Deși promisiunea este mare, există și provocări. Specificitatea țintirii EPAC, fără a perturba alte căi cAMP-dependente (cum ar fi cele mediate de PKA), este esențială pentru a evita efectele secundare nedorite. De asemenea, complexitatea semnalizării EPAC, cu acțiuni rapide și dependente de microdomeniu, necesită o înțelegere aprofundată pentru a proiecta terapii eficiente. Cu toate acestea, progresele înregistrate în identificarea și caracterizarea compușilor care modulează EPAC sunt încurajatoare și sugerează un viitor promițător pentru EPAC ca țintă terapeutică în bolile cardiovasculare.
Întrebări Frecvente Despre EPAC și Sănătatea Inimii
- Ce este diferența principală între EPAC și PKA?
- Ambele sunt activate de cAMP, dar PKA acționează prin fosforilarea proteinelor, în timp ce EPAC este un factor de schimb de nucleotide guanină (GEF) pentru proteinele Ras, în special Rap1, declanșând căi de semnalizare distincte. EPAC activează direct Rap1, spre deosebire de PKA care fosforilează substraturi.
- Cum contribuie EPAC la hipertrofia cardiacă?
- EPAC activează cuplarea excitație-transcripție prin creșterea nivelurilor de Ca2+ în nucleoplasmă, ducând la translocarea histon-deacetilazei (HDAC) din nucleu și de-represia factorului de transcripție MEF2, care promovează creșterea cardiomiocitelor.
- EPAC este întotdeauna dăunător pentru inimă?
- Nu neapărat. Textul menționează că EPAC "integrează semnale pro- și anti-fibrotice". Rolul său este complex și depinde de context (tipul de celulă, durata și intensitatea activării, prezența altor semnale). Deși poate contribui la patologii precum fibroza și aritmiile, în anumite condiții, ar putea avea și roluri adaptative sau protectoare, de aceea este un domeniu de cercetare activ.
- Ce înseamnă "cuplarea excitație-contracție" și "cuplarea excitație-transcripție"?
- Cuplarea excitație-contracție este procesul prin care un impuls electric (excitație) declanșează eliberarea de calciu și, ulterior, contracția celulei musculare cardiace. Cuplarea excitație-transcripție este procesul prin care semnalele de calciu (excitația) reglează expresia genelor (transcripția), influențând astfel adaptările structurale și funcționale ale inimii pe termen lung.
- Există deja medicamente care țintesc EPAC?
- Nu există medicamente aprobate clinic care să țintească direct EPAC. Cu toate acestea, cercetările sunt în curs de desfășurare, iar în laborator au fost dezvoltate analogi specifici (agoniști) și inhibitori ai EPAC, folosiți pentru studii preclinice și pentru a înțelege mai bine rolul său în boală.
În concluzie, EPAC este un regulator dinamic și versatil al funcției cardiace, cu un impact semnificativ asupra homeostaziei calciului, cuplării excitație-contracție și excitație-transcripție, hipertrofiei și, în mod direct, a fibrozei. Capacitatea sa de a integra semnale pro- și anti-fibrotice îl face o țintă de cercetare fascinantă. Pe măsură ce înțelegerea noastră asupra acestui efector de AMP ciclic avansează, la fel crește și potențialul de a dezvolta strategii terapeutice noi și țintite pentru a combate bolile cardiovasculare, inclusiv fibroza cardiacă, o cauză majoră a morbidității și mortalității la nivel mondial. Este clar că EPAC nu este doar un simplu mesager, ci un orchestrator complex al răspunsurilor inimii la stres și boală, deschizând noi orizonturi în cardiologia modernă.
Dacă vrei să descoperi și alte articole similare cu EPAC și Fibroza Cardiacă: O Legătură Vitală, poți vizita categoria Sănătate.